從最初的技術(shù)積累與商業(yè)模式探索,到臨床前候選藥物與藥物管線(xiàn)的驗(yàn)證交付,在經(jīng)歷近十年的發(fā)展后,數(shù)十家人工智能(AI)+藥物研發(fā)型企業(yè)在國(guó)內(nèi)陸續(xù)成立。
一個(gè)工業(yè)賽道在短時(shí)間內(nèi)忽然變得擁擠。AI技術(shù)加入醫(yī)藥研發(fā)的主要原因是醫(yī)藥工業(yè)的研發(fā)成本已經(jīng)到了難以容忍的程度, 同時(shí)隨著人工智能技術(shù)的不斷成熟,為AI進(jìn)入醫(yī)藥研發(fā)流程帶來(lái)了一批新的生力軍, 如AI專(zhuān)家,計(jì)算機(jī)硬件工程師等。這批醫(yī)藥工業(yè)的新人雖然不具有醫(yī)藥工業(yè)的研發(fā)知識(shí),但他們將把一批全新的技術(shù)和思維帶入了醫(yī)藥工業(yè)。
在如今這一嶄新的醫(yī)藥研發(fā)領(lǐng)域,AI技術(shù)催生出了哪些新商業(yè)模式?AI技術(shù)在賦能藥物研發(fā)中究竟覆蓋了哪些應(yīng)用場(chǎng)景?由AI技術(shù)賦能的藥物研發(fā)都推進(jìn)到了哪個(gè)階段?AI+藥物研發(fā)企業(yè)在激烈競(jìng)爭(zhēng)下,未來(lái)的突破口可能又在哪里?
為了進(jìn)一步了解我國(guó)AI+藥物研發(fā)企業(yè)的發(fā)展進(jìn)程,動(dòng)脈網(wǎng)近期以藥物研發(fā)流程為導(dǎo)向,選取了該賽道74家企業(yè)進(jìn)行盤(pán)點(diǎn)分析。
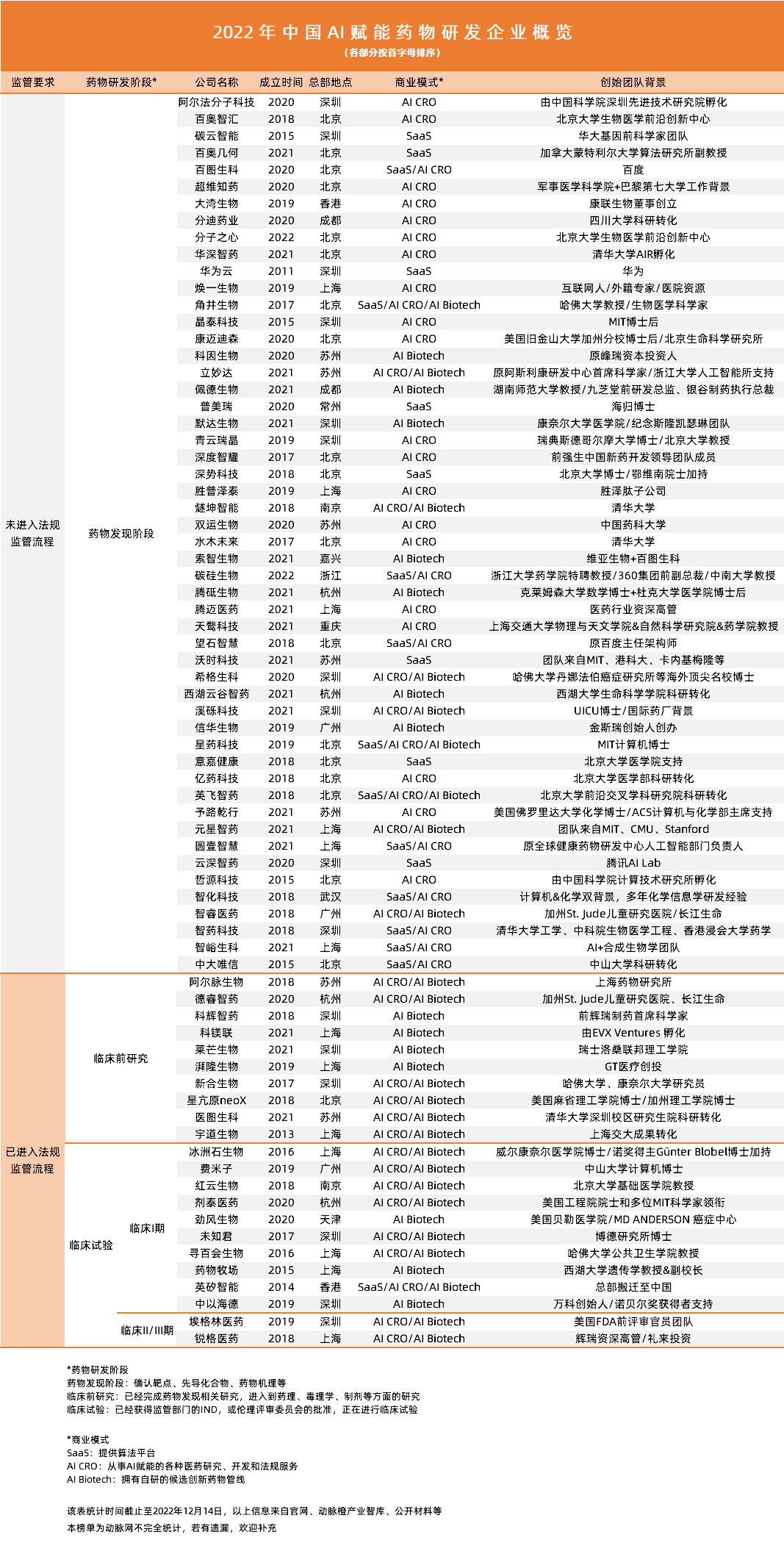
從SaaS到AI CRO,再到AI Biotech,商業(yè)演化反應(yīng)行業(yè)進(jìn)化
2014-2017年,我國(guó)第一批AI+藥物研發(fā)企業(yè)成立,AI技術(shù)在藥物研發(fā)行業(yè)的技術(shù)開(kāi)發(fā)與商業(yè)模式探索隨之展開(kāi)。該時(shí)期的企業(yè)主要通過(guò)提供AI計(jì)算工具來(lái)輔助藥物開(kāi)發(fā),SaaS服務(wù)為該時(shí)期的典型商業(yè)模式。
2018-2019年,最早一批AI+新藥企業(yè)基本完成前期技術(shù)積累,并陸續(xù)開(kāi)始獲得臨床前候選藥物(Pre-clinical candidate, PCC)一類(lèi)的驗(yàn)證性成果。這一時(shí)期,部分AI+藥物研發(fā)企業(yè)為藥企或藥物研發(fā)CRO企業(yè)提供更具廣度和深度的端到端AI技術(shù)服務(wù)。一種新的商業(yè)模式開(kāi)始出現(xiàn):AI+CRO。
2020年后,行業(yè)進(jìn)入快速發(fā)展階段,賽道開(kāi)始逐步擁擠。AI+新藥企業(yè)與藥企的合作頻次、合作范圍、合作深度不斷拓展,部分AI+藥物研發(fā)企業(yè)也開(kāi)始進(jìn)行獨(dú)立的藥物管線(xiàn)全流程應(yīng)用與開(kāi)發(fā),即商業(yè)模式為AI Biotech的企業(yè)開(kāi)始出現(xiàn)。
至此,SaaS、AI CRO與AI Biotech,成為我國(guó)目前AI+新藥企業(yè)的三種主要商業(yè)模式。這三種商業(yè)模式的發(fā)展演化,也從側(cè)面放映了我國(guó)AI+藥物研發(fā)企業(yè)的發(fā)展。
藥物發(fā)現(xiàn)階段企業(yè)占70%,僅有兩家企業(yè)的自有候選藥物進(jìn)入中晚期臨床試驗(yàn)
落實(shí)到新藥的研發(fā)流程,主要包含藥物發(fā)現(xiàn)階段、臨床前研究(藥理和毒理為主)和臨床試驗(yàn)三個(gè)階段,其中除藥物發(fā)現(xiàn)階段外,后續(xù)兩個(gè)階段均受到不同程度的法規(guī)監(jiān)管。例如:某一款候選藥物在幾只動(dòng)物體內(nèi)引起的神經(jīng)毒性或腎毒性足以讓監(jiān)管機(jī)構(gòu)拒絕該候選藥物進(jìn)入一期臨床試驗(yàn)。而臨床上的任何試驗(yàn)程序,倫理和設(shè)計(jì)都必須受到監(jiān)管機(jī)構(gòu)的嚴(yán)格監(jiān)控。
根據(jù)動(dòng)脈網(wǎng)統(tǒng)計(jì),目前我國(guó)AI+藥物研發(fā)企業(yè)中,約70%企業(yè)的業(yè)務(wù)處于藥物發(fā)現(xiàn)階段,而進(jìn)入到臨床前研究階段和臨床試驗(yàn)階段的企業(yè)僅占約15%。
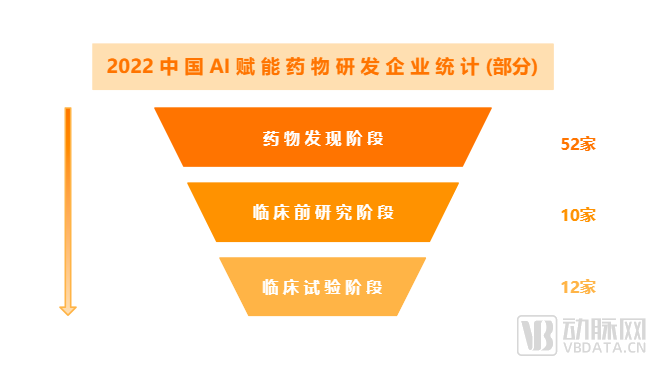
總體來(lái)說(shuō),從藥物發(fā)現(xiàn)到臨床試驗(yàn),我國(guó)AI技術(shù)賦能藥物研發(fā)在技術(shù)層面已經(jīng)逼近“終點(diǎn)”,“跑得較快”的企業(yè)已經(jīng)進(jìn)入到中后期臨床試驗(yàn)階段。
1、藥物發(fā)現(xiàn):SaaS、AI CRO企業(yè)主導(dǎo),比算法、比交付
從具體研發(fā)流程來(lái)看,在最基礎(chǔ)的藥物發(fā)現(xiàn)階段,主要分為:藥物靶點(diǎn)以及生物標(biāo)志物的選擇與確認(rèn)、先導(dǎo)化合物的確認(rèn)、構(gòu)效關(guān)系的研究與活性化合物的篩選、臨床前候選藥物(PCC)的選定,4項(xiàng)步驟。
針對(duì)該階段的相應(yīng)步驟,AI技術(shù)目前發(fā)展較為成熟的應(yīng)用場(chǎng)景包括:虛擬篩選、分子生成、靶點(diǎn)發(fā)現(xiàn)及驗(yàn)證、ADMET預(yù)測(cè)、藥物重定向等,提供相應(yīng)技術(shù)的企業(yè)主要以SaaS、AI CRO,以及SaaS與AI CRO混合商業(yè)模式為主。同時(shí)也有近兩年剛剛成立的Biotech企業(yè)。
以SaaS服務(wù)模式提供AI輔助藥物開(kāi)發(fā)算法平臺(tái)的企業(yè),其創(chuàng)始團(tuán)隊(duì)大多是在計(jì)算機(jī)算法、物理、數(shù)學(xué)等領(lǐng)域的高精尖人才,或者是由百度、華為、騰訊等大廠(chǎng)親自“下場(chǎng)”搭建。例如百圖生科、華為云ElHealth、云深智藥、碳云智能、深勢(shì)科技、星藥科技等。
該種商業(yè)模式下,搭建算得更準(zhǔn)的算法模型、開(kāi)發(fā)考慮更全的結(jié)構(gòu)模擬、迭代通量更高的虛擬篩選、提供操作更簡(jiǎn)的使用感受等,是企業(yè)間始終在自我突破、互相競(jìng)爭(zhēng)的幾個(gè)方面。
以AI CRO為主要商業(yè)模式的企業(yè),大部分是著名高校的科研成果轉(zhuǎn)化而來(lái),例如華深智藥、立妙達(dá)、燧坤智能、英飛智藥、天鶩科技等,也有以晶泰科技為代表的由世界名校博士創(chuàng)建的企業(yè)。不同于計(jì)算服務(wù)提供商,該類(lèi)企業(yè)擅長(zhǎng)的是發(fā)現(xiàn)成藥靶點(diǎn)、先導(dǎo)化合物或PCC,并將此部分研究成果面向藥企等進(jìn)行商業(yè)轉(zhuǎn)化,合作推進(jìn)藥物研發(fā)管線(xiàn)。
部分AI CRO企業(yè)采取與SaaS企業(yè)進(jìn)行合作的形式,結(jié)合雙方的技術(shù)優(yōu)勢(shì),投入更多的技術(shù)與時(shí)間到PCC發(fā)現(xiàn),以及與藥企合作管線(xiàn)的推進(jìn)中。經(jīng)過(guò)積累,在未來(lái),這部分企業(yè)也是非常有潛力開(kāi)設(shè)自研藥物管線(xiàn)的。
同時(shí),在這一階段也有部分SaaS企業(yè)近年來(lái)開(kāi)始向AI CRO模式進(jìn)行探索。以圓壹智慧、智峪生科為例,這部分企業(yè)主要優(yōu)勢(shì)在于其十分注重“AI+BT”的復(fù)合型人才團(tuán)隊(duì),由此激發(fā)了企業(yè)的更多可能性。
2、臨床前研究:AI CRO、AI Biotech主導(dǎo),比IND獲批的成熟度、差異化
繼藥物發(fā)現(xiàn)之后,藥物研發(fā)開(kāi)始進(jìn)入法規(guī)監(jiān)管流程,包括臨床前研究和臨床試驗(yàn)兩個(gè)階段。
在臨床前研究階段,需要經(jīng)過(guò)CMC、藥代動(dòng)力學(xué)評(píng)估、安全性藥理研究、毒理研究、制劑開(kāi)發(fā),5項(xiàng)主要工作,目的是對(duì)PCC進(jìn)行驗(yàn)證,評(píng)估其可轉(zhuǎn)化性。
本階段主要包含AI CRO和AI Biotech兩種商業(yè)模式。區(qū)別于藥物發(fā)現(xiàn)階段的AI CRO企業(yè),在臨床前研究階段的AI CRO企業(yè)不僅能夠完成PCC發(fā)現(xiàn),同時(shí)還需要將PCC進(jìn)行多維度的實(shí)驗(yàn)評(píng)估驗(yàn)證,以證明其是具備進(jìn)入臨床IND申報(bào)的有效化合物。
總體而言,AI Biotech是該階段的主要商業(yè)模式,即其自有管線(xiàn)目前已經(jīng)完成藥物發(fā)現(xiàn),確定了PCC,即將或正在進(jìn)行IND申報(bào)。這部分企業(yè)大多在2018年后成立,這意味著僅約3年時(shí)間即可確認(rèn)PCC,完全證明了AI技術(shù)在藥物發(fā)現(xiàn)階段的技術(shù)可行性。尤其是科鎂聯(lián)、醫(yī)圖生科等剛剛成立的企業(yè),就已經(jīng)進(jìn)入到了進(jìn)入IND申報(bào)的階段,AI技術(shù)對(duì)藥物開(kāi)發(fā)“降本增效”的更大潛力,足以想見(jiàn)。
3、臨床試驗(yàn):AI Biotech主導(dǎo),比合規(guī)、比進(jìn)度、比臨床試驗(yàn)成功率
當(dāng)化合物通過(guò)了臨床前實(shí)驗(yàn)后,需要相關(guān)藥檢部門(mén)通過(guò)IND申請(qǐng),或獲得倫理評(píng)審委員會(huì)的批注,方可展開(kāi)I期臨床試驗(yàn)。
可喜的是,我國(guó)目前已經(jīng)有12家AI Biotech企業(yè)將自研管線(xiàn)從藥物發(fā)現(xiàn)推進(jìn)到了臨床試驗(yàn)階段,其中10家處于I期臨床,2家已經(jīng)進(jìn)入到了中后期臨床試驗(yàn)。這部分企業(yè)半數(shù)為成立于2014-2017年的第一批AI+藥物研發(fā)企業(yè)。
值得注意的是,很多這樣的企業(yè)在創(chuàng)始團(tuán)隊(duì)中均擁有來(lái)自海外高校、研究機(jī)構(gòu)或大型藥企的相關(guān)人才或支持。盡管全球范圍內(nèi)目前尚無(wú)AI賦能研發(fā)的藥物獲批上市,但相較于國(guó)內(nèi),AI技術(shù)賦能藥物研發(fā)在國(guó)外起步更早,進(jìn)入到臨床試驗(yàn)階段的企業(yè)更多,可參考借鑒的經(jīng)驗(yàn)也就更豐富。
之所以這一階段需要參考經(jīng)驗(yàn)與多元支持,是因?yàn)榕R床試驗(yàn)階段的失敗率極高。眾所周知,I期臨床試驗(yàn)的主要目的是確定藥品的安全性。大約60%的候選藥品在這個(gè)階段失敗。失敗的主要原因包括:體內(nèi)毒性過(guò)高,藥物的“安全窗”過(guò)小,以及主要靶器官出現(xiàn)的不可逆毒性。有人稱(chēng)這部分試驗(yàn)是醫(yī)藥研發(fā)的“死亡之谷”。
提升臨床試驗(yàn)階段的推進(jìn)速度、選擇合適的藥效評(píng)價(jià)模型、判定合理的適應(yīng)癥應(yīng)用、制定合規(guī)的臨床試驗(yàn)計(jì)劃,每一步都十分重要,不僅需要企業(yè)有過(guò)硬的AI和藥物研發(fā)能力,更是考驗(yàn)企業(yè)在這一高監(jiān)管階段對(duì)于相關(guān)法規(guī)注冊(cè)程序和關(guān)鍵點(diǎn)的熟悉和理解,以及開(kāi)展臨床試驗(yàn)的能力。
目前進(jìn)入到中后期臨床的企業(yè)共兩家,一個(gè)是擁有美國(guó)FDA前評(píng)審官員團(tuán)隊(duì)的埃格林醫(yī)藥,一個(gè)是擁有輝瑞和禮來(lái)雙重支持的銳格醫(yī)藥。兩家企業(yè)積累的雖然是“監(jiān)管機(jī)構(gòu)”和“頂尖藥企”兩種不同角色的行業(yè)經(jīng)驗(yàn),都在管線(xiàn)的中后期推進(jìn)上二者皆取得了突出的階段性成果。目前,埃格林醫(yī)藥已有2條管線(xiàn)進(jìn)入到臨床中后期,銳格醫(yī)藥也宣布參與其一項(xiàng)II臨床試驗(yàn)的受試者已于今年四月開(kāi)始入組。
同時(shí)也必須指出,開(kāi)發(fā)有迫切臨床需求的候選藥品是任何進(jìn)入II期臨床藥品的關(guān)鍵。例如,埃格林開(kāi)發(fā)的兩款創(chuàng)新候選藥品,一款是用于治療眼底干性黃斑病變,一款是用于治療產(chǎn)科的先兆子癇。而上述兩個(gè)臨床適應(yīng)癥目前均屬于無(wú)藥可治的臨床疾患。中國(guó)醫(yī)藥工業(yè)已經(jīng)被那種數(shù)十個(gè),甚至上百個(gè)某種First in Class的候選藥品的現(xiàn)象困擾已久,“候選冠軍”也會(huì)因?yàn)檫t遲無(wú)法完成臨床轉(zhuǎn)化而面臨失去意義的風(fēng)險(xiǎn)。
AI應(yīng)用場(chǎng)景向后延伸,加速進(jìn)入監(jiān)管流程是趨勢(shì)也是必然
回顧AI技術(shù)賦能我國(guó)藥物研發(fā)的近十年,伴隨商業(yè)模式的不斷演化,也反映出我國(guó)創(chuàng)新藥企業(yè)在A(yíng)I+藥物研發(fā)這一賽道上越跑越寬、越跑越遠(yuǎn)的良好態(tài)勢(shì)。
傳統(tǒng)藥企和互聯(lián)網(wǎng)大廠(chǎng)的入局使得這條賽道近年來(lái)愈發(fā)擁擠,特別是在進(jìn)入藥品監(jiān)管前的藥物發(fā)現(xiàn)階段,競(jìng)爭(zhēng)在日益加劇。長(zhǎng)遠(yuǎn)來(lái)看,AI制藥的CRO模式會(huì)趨于同質(zhì)化,親自下場(chǎng)做藥會(huì)是提高企業(yè)附加值的商業(yè)模式,當(dāng)然也是對(duì)企業(yè)的人工智能研發(fā)能力、藥物臨床能力及法規(guī)理解能力的多重考驗(yàn)。橫向來(lái)看,企業(yè)間相互競(jìng)爭(zhēng)的是市場(chǎng)、是速度、是準(zhǔn)度。縱向而言,加速藥物管線(xiàn)的切實(shí)推進(jìn),以及打通AI技術(shù)在全藥物研發(fā)流程的應(yīng)用場(chǎng)景,考驗(yàn)得更多的是企業(yè)的“端到端”能力。
面臨如此多維度的挑戰(zhàn),將AI技術(shù)“降本增效”的優(yōu)勢(shì)輻射至整個(gè)藥物研發(fā)流程,實(shí)現(xiàn)更多的“First in Class”、“Best in Class”的藥物獲批上市,SaaS、AI CRO和AI Biotech企業(yè)的目標(biāo)始終不曾改變,腳步從未停下。
放眼全球,AI對(duì)臨床前研究和臨床試驗(yàn)方面的技術(shù)探索也已經(jīng)起步。劑型設(shè)計(jì)、新形態(tài)藥物遞送、臨床患者分層、臨床試驗(yàn)設(shè)計(jì)優(yōu)化、臨床結(jié)果預(yù)測(cè)、虛擬臨床試驗(yàn)、真實(shí)世界研究等新的AI技術(shù)應(yīng)用場(chǎng)景開(kāi)始出現(xiàn)。
不難預(yù)測(cè),未來(lái)不論是AI技術(shù)的應(yīng)用探索,還是AI+藥物研發(fā)企業(yè)的發(fā)展重心,均會(huì)逐漸延伸至受法規(guī)監(jiān)管的臨床前研究和臨床試驗(yàn)階段。
伴隨AI技術(shù)的發(fā)展與滲透,憑借行業(yè)內(nèi)對(duì)“快速推進(jìn)藥物研發(fā)”的堅(jiān)定追求,我們已經(jīng)到了可以期待AI藥物上市的時(shí)候!
文章轉(zhuǎn)載自動(dòng)脈網(wǎng),更多信息請(qǐng)閱讀原文